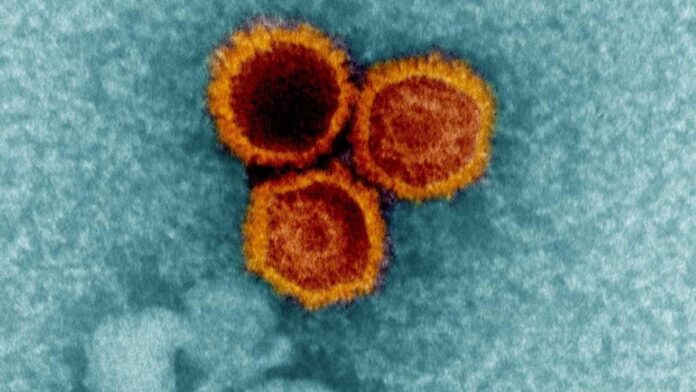
De plus en plus de preuves indiquent que le virus Epstein-Barr (EBV) – l’un des virus les plus répandus au monde – est un déclencheur clé de la sclérose en plaques (SEP), une maladie auto-immune débilitante. Pendant des décennies, les scientifiques soupçonnaient un lien, mais de nouvelles recherches révèlent maintenant comment le virus pourrait être à l’origine du développement de la maladie.
L’EBV omniprésent et son rôle mystérieux
L’EBV, responsable de la mononucléose infectieuse (« maladie du baiser »), infecte environ 95 % de la population adulte. Il persiste dans l’organisme, parfois même caché dans les cellules du cerveau, longtemps après l’exposition initiale. La corrélation frappante entre l’infection par l’EBV et la SEP est connue depuis un certain temps : les personnes atteintes de SEP sont presque universellement testées positives pour une exposition antérieure à l’EBV. Une étude historique menée en 2022 auprès de plus de 10 millions de personnes a révélé que le risque de SEP augmente 32 fois après une infection par l’EBV – un lien bien plus fort que tout autre virus testé.
Les cellules T tueuses comme pièce manquante
Des chercheurs de l’Université de Californie à San Francisco (UCSF) ont désormais identifié un mécanisme plausible à l’origine de ce lien. Leurs travaux récents montrent que les lymphocytes T « tueurs » – des cellules immunitaires conçues pour détruire les cellules infectées – sont nettement plus abondants chez les patients atteints de SEP. Il est important de noter que bon nombre de ces lymphocytes T sont spécifiquement activés contre les protéines EBV.
“L’examen de ces cellules T CD8+ peu étudiées relie de nombreux points différents et nous donne une nouvelle fenêtre sur la manière dont l’EBV contribue probablement à cette maladie”, explique le neurologue Joe Sabatino de l’UCSF. Cela suggère que le système immunitaire attaque par erreur les propres fibres nerveuses du corps après avoir été amorcé par le virus.
Preuves provenant du sang et du liquide céphalo-rachidien
L’équipe de l’UCSF a analysé le sang et le liquide céphalorachidien (LCR) de 13 patients atteints de SEP et les a comparés à 5 témoins (y compris ceux souffrant d’autres maladies inflammatoires). Les résultats ont été frappants : les lymphocytes T tueurs réactifs à l’EBV étaient jusqu’à 100 fois plus concentrés dans le LCR des patients atteints de SEP que dans leur sang. Cela indique une réponse immunitaire agressive se produisant dans le cerveau et la moelle épinière.
De plus, des gènes actifs de l’EBV ont été détectés dans le LCR de patients atteints de SEP – gènes absents ou inactifs chez les personnes non atteintes de la maladie. Un gène, en particulier, était exclusivement actif chez les patients atteints de SEP, ce qui suggère que le virus n’est pas simplement présent mais qu’il se réactive dans le système nerveux central.
Implications plus larges pour les maladies à médiation immunitaire
Les implications s’étendent au-delà de la SEP. L’EBV est de plus en plus lié à d’autres maladies auto-immunes et neurologiques, notamment le lupus, certains cancers, la schizophrénie, la COVID longue, le syndrome de fatigue chronique et même la démence. Comprendre comment l’EBV manipule le système immunitaire pourrait débloquer des traitements pour un large éventail de maladies.
« Le grand espoir ici est que si nous parvenons à interférer avec l’EBV, nous pourrons avoir un effet important, non seulement sur la SEP mais sur d’autres troubles, et améliorer la qualité de vie d’un très grand nombre de personnes », déclare Sabatino.
Interférer avec l’EBV pourrait conduire à des avancées majeures dans le traitement de nombreuses maladies, et pas seulement de la SEP. Le rôle du virus dans le dysfonctionnement immunitaire devient plus clair et les futures thérapies pourraient se concentrer sur le contrôle ou la suppression de l’activité de l’EBV afin de prévenir ou d’atténuer ces conditions.