Naukowcy odkryli, że antybiotyki aminoglikozydowe, ważna klasa leków stosowanych w leczeniu ciężkich infekcji bakteryjnych, przenikają do bakterii nie poprzez bierną dyfuzję, ale poprzez przejmowanie transporterów cukru. Odkrycie to, opublikowane w czasopiśmie Science Advances 5 września 2025 r. przez naukowców z Instytutu Pasteura i instytucji z nim stowarzyszonych, może zrewolucjonizować strategie leczenia antybiotykami, szczególnie w obliczu rosnącej oporności na antybiotyki.
Długo rozwiązana tajemnica przenikania antybiotyków
Przez dziesięciolecia nie było jasne, w jaki sposób aminoglikozydy pokonują mechanizmy obronne bakterii. Antybiotyki te skutecznie zabijają bakterie, takie jak Escherichia coli, Pseudomonas aeruginosa i Staphylococcus aureus, blokując syntezę białek. Jednakże niektóre szczepy, w tym coraz bardziej oporny E. coli opracowała sposoby uniknięcia leczenia, co doprowadziło do szacunkowo 829 000 zgonów na całym świecie w 2019 r. Przeważająca teoria sugeruje, że aminoglikozydy biernie przenikają przez ścianę komórkową bakterii, ale nowe dowody sugerują coś innego.
Rola przewoźników cukru
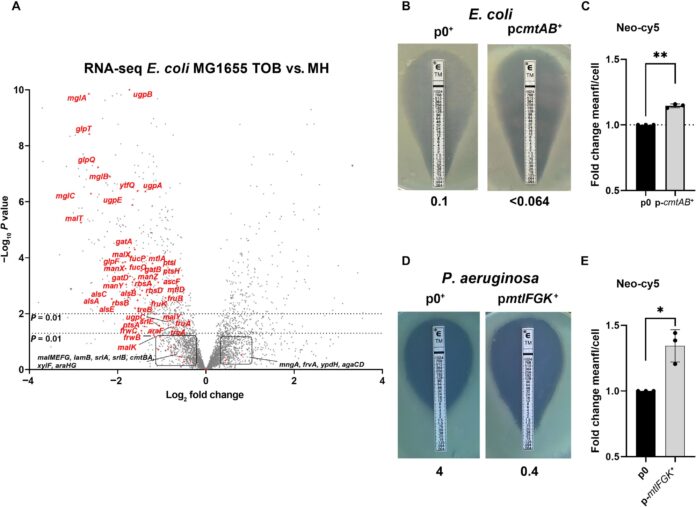
Naukowcy natknęli się na to odkrycie przez przypadek, badając reakcje bakterii na stres antybiotykowy u Vibrio cholerae. Odkryli korelację między skutecznością antybiotyku a obecnością transporterów cukru – bram molekularnych, których bakterie używają do importowania niezbędnych węglowodanów, takich jak glukoza, sacharoza i fruktoza. Zaintrygowani zbadali ten mechanizm w E. coli.
Korzystając z fluorescencyjnych aminoglikozydów, bezpośrednio obserwowali, w jaki sposób antybiotyki aktywnie przedostają się do komórek bakteryjnych za pośrednictwem tych transporterów cukru. Po raz pierwszy udowodniono, że antybiotyk wykorzystuje ten środek transportu. „To było nieoczekiwane odkrycie” – wyjaśnia Zeynep Baharoğlu, główna autorka i dyrektor naukowa Instytutu Pasteura. „Ale dane były niezaprzeczalne”.
Zwiększanie skuteczności antybiotyków za pomocą urydyny
Zespół zdał sobie sprawę, że liczba transporterów cukru nie jest stała; ich liczba zmienia się w zależności od środowiska. Manipulując dostępnością niektórych cukrów, mogliby potencjalnie zwiększyć liczbę transporterów, a tym samym przepuszczalność antybiotyków.
Po sprawdzeniu 200 związków zidentyfikowali urydynę jako szczególnie skutecznego kandydata. Podobnie jak w przypadku próbek płynów ustrojowych człowieka zanieczyszczonych E. coli, a w zwierzęcych modelach infekcji dróg moczowych urydyna podwoiła liczbę transporterów cukru, co doprowadziło do dziesięciokrotnego wzrostu wrażliwości bakterii na aminoglikozydy. Warto zauważyć, że nawet szczepy lekooporne i wielolekooporne odzyskały wrażliwość w obecności urydyny.
Konsekwencje dotyczące oporności na antybiotyki i przyszłych metod leczenia
Odkrycie to ma daleko idące implikacje. Podając urydynę wraz z aminoglikozydami, lekarze mogą zmniejszyć dawki antybiotyków, minimalizując ryzyko dalszego rozwoju oporności i ograniczając toksyczne skutki uboczne. Wysokie dawki aminoglikozydów mogą powodować uszkodzenie ucha wewnętrznego i nerek, które można złagodzić, stosując mniejsze dawki.
„To ważne odkrycie, które może zmienić zasady gry w przypadku tej klasy antybiotyków” – mówi Baharoglou. „Może to pozwolić nam na stosowanie niższych stężeń lub krótszych cykli leczenia, przedłużając użyteczność tych leków”.
Inną możliwością jest „przeszczepienie” urydyny na inne antybiotyki, aby zwiększyć ich penetrację przez oporne bakterie. Fakt, że urydyna jest już w zastosowaniu klinicznym i wykazano, że jest bezpieczna dla ludzi, może przyspieszyć rozwój i testowanie tych nowych strategii.
Krytyczny krok w walce z opornością na antybiotyki
Światowa Organizacja Zdrowia szacuje, że w 2019 r. bakterie oporne na antybiotyki były przyczyną ponad 6 milionów zgonów. Badanie to podkreśla znaczenie podstawowych badań naukowych w walce z tym rosnącym globalnym zagrożeniem. „Bez tych podstawowych badań to odkrycie, które mogłoby odegrać kluczową rolę w przyszłych strategiach zwalczania oporności na antybiotyki, nie byłoby możliwe” – podsumowuje Didier Mazel, kierownik Jednostki Plastyki Genomu Bakteryjnego w Instytucie Pasteura. Ten przełom daje nową nadzieję w walce z opornością na antybiotyki, odkrywając nowy mechanizm poprawy skuteczności istniejących leków.