Вчені виявили, що аміноглікозидні антибіотики, важливий клас препаратів проти важких бактеріальних інфекцій, проникають до бактерій не через пасивну дифузію, а шляхом захоплення транспортерів цукру. Це відкриття, опубліковане в журналі Science Advances 5 вересня 2025 року дослідниками з Інституту Пастера та дочірніх установ, має потенціал змінити стратегії лікування антибіотиками, особливо в умовах зростаючої стійкості до антибіотиків.
Давно розгадана таємниця проникнення антибіотиків
Десятиліттями залишалося незрозумілим, як аміноглікозиди долають захист бактерій. Ці антибіотики ефективно вбивають такі бактерії, як Escherichia coli, Pseudomonas aeruginosa і Staphylococcus aureus, блокуючи синтез білка. Однак деякі штами, включаючи дедалі більш стійкий E. coli розробили способи уникнути лікування, що призвело до приблизно 829 000 смертей у всьому світі в 2019 році. Переважаюча теорія припускала, що аміноглікозиди пасивно перетинають стінку бактеріальної клітини, але нові дані свідчать про інше.
Роль транспортерів цукру
Дослідники натрапили на це відкриття випадково, вивчаючи реакцію бактерій на антибіотичний стрес у Vibrio cholerae. Вони виявили кореляцію між ефективністю антибіотика та наявністю транспортерів цукру — молекулярних шлюзів, які бактерії використовують для імпорту необхідних вуглеводів, таких як глюкоза, сахароза та фруктоза. Зацікавлені, вони дослідили цей механізм у E. кишкова паличка.
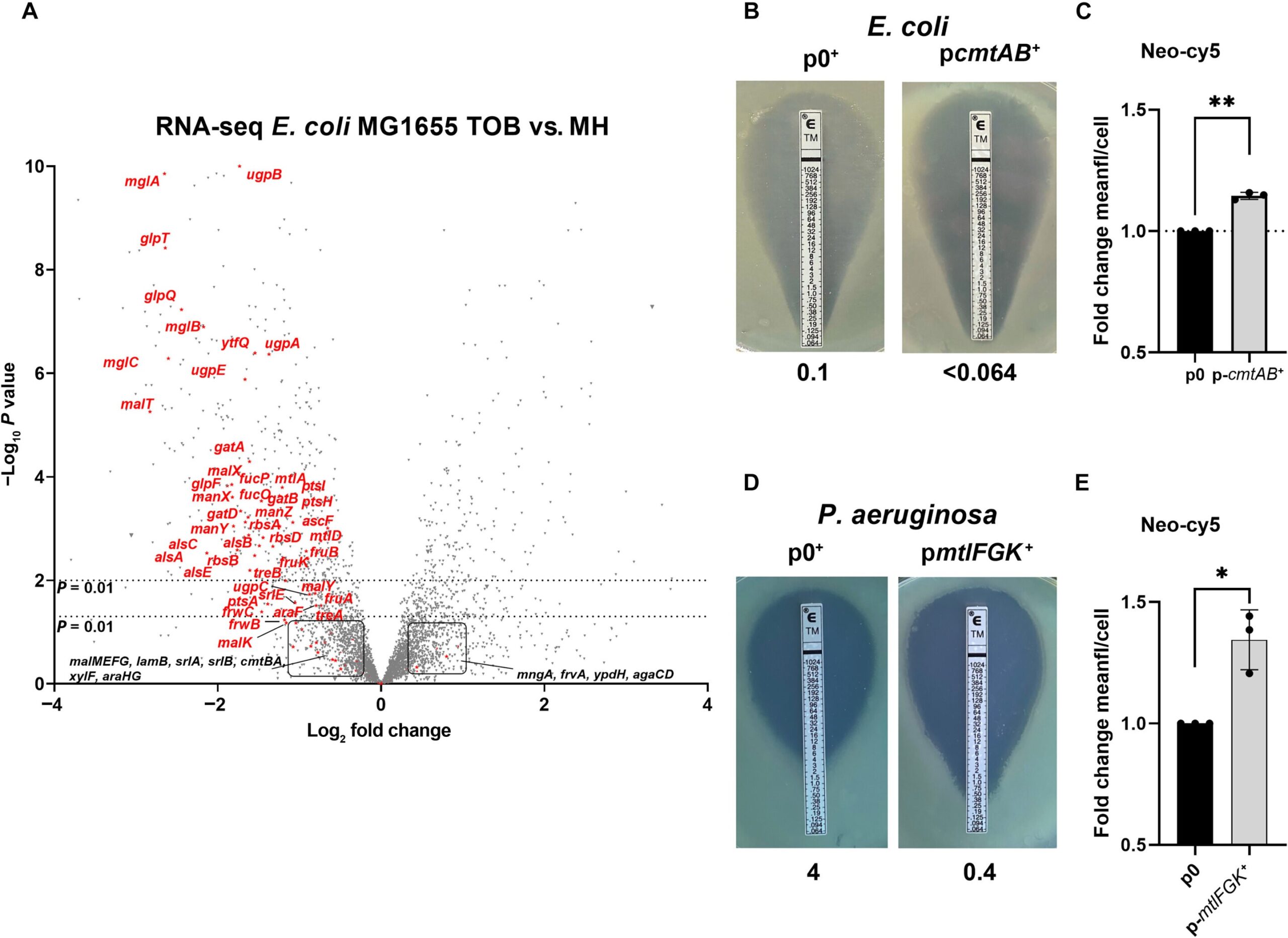
Використовуючи флуоресцентні аміноглікозиди, вони безпосередньо спостерігали, як антибіотики активно проникають у бактеріальні клітини через ці транспортери цукру. Це перший раз, коли було доведено, що антибіотик використовує цей вид транспорту. «Це було несподіване відкриття», — пояснює Зейнеп Багароглу, провідний автор і науковий директор Інституту Пастера. «Але дані були незаперечними».
Підвищення ефективності антибіотиків за допомогою уридину
Команда зрозуміла, що кількість транспортерів цукру не є фіксованою; їх кількість коливається в залежності від середовища. Маніпулюючи доступністю певних цукрів, вони потенційно можуть збільшити кількість транспортерів і, отже, проникність антибіотиків.
Після перевірки 200 сполук вони визначили уридин як особливо ефективний кандидат. Як і у зразках рідин людського тіла, забруднених E. coli та на тваринних моделях інфекцій сечовивідних шляхів уридин подвоїв кількість транспортерів цукру, що призвело до десятикратного підвищення чутливості бактерій до аміноглікозидів. Примітно, що навіть резистентні до ліків і мультирезистентні штами відновлювали чутливість у присутності уридину.
Наслідки для антибіотикорезистентності та майбутні методи лікування
Це відкриття має далекосяжні наслідки. Застосовуючи уридин разом з аміноглікозидами, клініцисти можуть зменшити дози антибіотиків, мінімізуючи ризик подальшого розвитку резистентності та зменшуючи токсичні побічні ефекти. Високі дози аміноглікозидів можуть спричинити пошкодження внутрішнього вуха та нирок, яке можна пом’якшити меншими дозами.
«Це важливе відкриття, яке може змінити правила гри для цього класу антибіотиків», — каже Багароглу. «Це може дозволити нам використовувати нижчі концентрації або коротші курси лікування, продовжуючи ефективність цих препаратів».
Інша можливість полягає в «щепленні» уридину іншим антибіотикам, щоб збільшити їх проникнення в стійкі бактерії. Той факт, що уридин вже використовується в клінічній практиці та доведено, що він безпечний для людей, може прискорити розробку та тестування цих нових стратегій.
Вирішальний крок у боротьбі зі стійкістю до антибіотиків
За оцінками Всесвітньої організації охорони здоров’я, у 2019 році стійкі до антибіотиків бактерії спричинили понад 6 мільйонів смертей. Це дослідження підкреслює важливість фундаментальних наукових досліджень у боротьбі з цією зростаючою глобальною загрозою. «Без цих фундаментальних досліджень це відкриття, яке могло б зіграти ключову роль у майбутніх стратегіях боротьби зі стійкістю до антибіотиків, було б неможливим», — підсумовує Дідьє Мазел, керівник відділу пластичності бактеріального геному в Інституті Пастера. Цей прорив дає нову надію в боротьбі зі стійкістю до антибіотиків, відкриваючи новий механізм підвищення ефективності існуючих ліків.