Un uomo norvegese di 63 anni, indicato nella letteratura medica come il “paziente di Oslo”, ha raggiunto un traguardo raro e significativo: la remissione a lungo termine dall’HIV. A seguito di un trapianto di midollo osseo da parte di suo fratello, il paziente ha mantenuto uno stato privo di virus per cinque anni senza la necessità di farmaci antiretrovirali giornalieri.
Sebbene questo caso fornisca una tabella di marcia vitale per gli scienziati, mette in luce sia l’incredibile potenziale della ricerca genetica sia i rischi medici estremi coinvolti in tali procedure.
Il meccanismo di resistenza: la mutazione CCR5
La chiave di questo successo risiede in una specifica stranezza genetica. Durante il trattamento del paziente per un raro cancro del sangue, i ricercatori hanno scoperto che suo fratello possedeva una rara mutazione nota come CCR5Δ32/Δ32.
Per capire perché questo è importante, bisogna guardare come opera l’HIV:
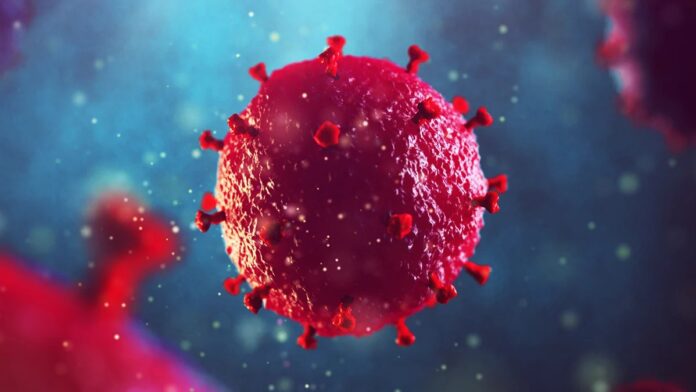
– L’HIV tipicamente entra nelle cellule immunitarie umane legandosi a un recettore specifico chiamato CCR5.
– La mutazione Δ32 “elimina” effettivamente questi recettori dai globuli bianchi.
– Senza questo punto di ingresso, il virus non può penetrare nelle cellule, rendendo il sistema immunitario funzionalmente impermeabile all’HIV.
Ricevendo un trapianto di cellule staminali da suo fratello, il paziente di Oslo ha sostituito il suo sistema immunitario suscettibile con uno geneticamente protetto dal virus.
Perché questo caso è scientificamente significativo
Sebbene nella storia della medicina siano state documentate diverse “cure funzionali”, il caso del paziente di Oslo offre dati unici che lo distinguono dagli altri:
1. Ripulire il “serbatoio virale”
La sfida più grande nella cura dell’HIV è la capacità del virus di nascondersi in “serbatoi” – sacche dormienti di DNA all’interno del corpo che i farmaci non possono raggiungere. La maggior parte dei casi di remissione si scontra con il fatto che il virus persiste nell’intestino. Tuttavia, test approfonditi sul paziente di Oslo hanno dimostrato che il DNA dell’HIV funzionante è stato eliminato anche dall’intestino, che è dove il virus si annida più comunemente.
2. La memoria biologica che svanisce
I ricercatori hanno osservato un fenomeno sorprendente: quando il virus è scomparso, il sistema immunitario del paziente ha smesso di reagire. Le cellule T specifiche dell’HIV sono diminuite e i livelli di anticorpi sono diminuiti. Ciò suggerisce che una volta che il virus è stato veramente debellato, anche la “memoria” dell’infezione da parte del corpo svanisce, una scoperta che aiuta gli scienziati a comprendere i marcatori biologici a lungo termine di una cura efficace.
3. Il ruolo delle reazioni immunitarie
Il paziente ha manifestato la malattia del trapianto contro l’ospite (GVHD), una condizione in cui le cellule del donatore attaccano il corpo del ricevente. È interessante notare che i ricercatori ritengono che questa intensa reazione immunitaria, insieme ai farmaci usati per trattarla, possa aver avuto un ruolo nel contribuire a “cancellare” le tracce rimanenti del virus.
Il confronto con la realtà: una cura contro un trattamento
È fondamentale distinguere tra una scoperta scientifica e una soluzione medica pratica.
Un trapianto di midollo osseo non è un percorso praticabile verso una cura diffusa dell’HIV per diversi motivi:
– Alto rischio: questi trapianti sono “riavvii del sistema immunitario” che comportano un tasso di mortalità del 10–20% entro il primo anno.
– Complessità: Si tratta di procedure ad alta intensità riservate ai tumori del sangue potenzialmente letali, non alla gestione delle infezioni virali croniche.
– Specificità: Una cura tramite questo metodo richiede un donatore con una mutazione genetica rara e molto specifica.
Guardando al futuro
L’obiettivo per la comunità scientifica non è eseguire più trapianti, ma estrarre dei “progetti” da questi rari casi. Analizzando i biomarcatori e i meccanismi molecolari presenti nel paziente di Oslo e in altri come lui, i ricercatori sperano di sviluppare terapie più sicure e accessibili – come l’editing genetico – che possano imitare questa resistenza naturale senza la necessità di un intervento chirurgico ad alto rischio.
Conclusione
Il paziente di Oslo offre uno sguardo raro su come appare una cura funzionale per l’HIV a livello cellulare. Sebbene il metodo di trapianto in sé sia troppo pericoloso per un uso generale, le conoscenze genetiche acquisite da questo caso sono essenziali per lo sviluppo di trattamenti futuri più sicuri che mirano a eliminare la capacità del virus di nascondersi e rimbalzare.